Los adenovirus aviares (FAdV) son virus que se han asociado con diferentes entidades clínicas en aves de corral; pueden causar diversas enfermedades en aves, incluyendo la hepatitis por cuerpos de inclusión (HCI), el síndrome de hepatitis-hidropericardio (SHH) y la erosión de molleja. Desde hace varias décadas, se encuentran entre un grupo de agentes infecciosos con gran impacto sobre la industria avícola a nivel global.
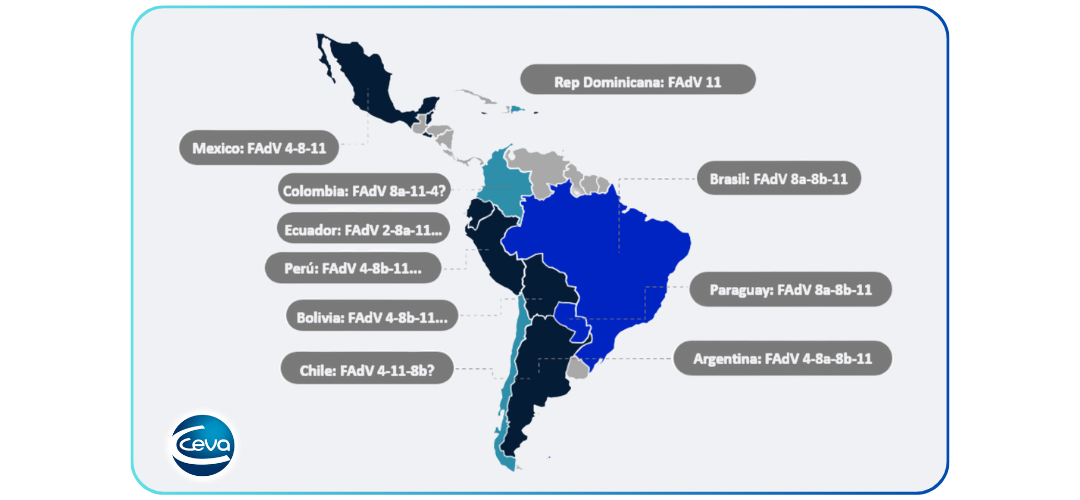
Los adenovirus aviares (FAdV) han sido detectados en varios países de Latinoamérica como patógenos emergentes, desde México hasta Argentina. Los principales genotipos detectados son FAdV-E, FAdV-C y FAdV-D, mientras que los serotipos más prevalentes son FAdV-4, FAdV-8b y FAdV-11; no obstante, también existen antecedentes de otros serotipos circulantes en algunos países o áreas de la región.

El impacto de cada serotipo puede variar significativamente; incluso se han caracterizado aislamientos con diferente virulencia perteneciente al mismo serotipo, lo cual determina las consecuencias de la enfermedad en términos de morbilidad y mortalidad. El serotipo 4 de FAdV está fuertemente asociado con el síndrome de hepatitis-hidropericardio, con alto impacto sobre la viabilidad de pollos de engorde. Otros serotipos, principalmente FAdV-8b, FAdV-11 y FAdV-8a, están relacionados con la hepatitis por cuerpos de inclusión, con impacto variable sobre los lotes de pollos afectados. Finalmente, se ha detectado el serotipo FAdV-1 relacionado con cuadros de erosión de molleja, una entidad sin gran impacto sobre la viabilidad de las aves, pero con graves consecuencias sobre el desempeño de los lotes (menor ganancia diaria de peso, menor eficiencia de conversión alimenticia y alta desuniformidad).
Además de las consecuencias clínicas específicas de cada serotipo, es importante considerar el impacto de las infecciones por FAdV sobre la inmunocompetencia de las aves, debido a que tienen la capacidad de reducir la respuesta inmune humoral y mediada por células a diversos antígenos y vacunas. Esto significa que las aves infectadas pueden tener una respuesta inmune disminuida frente a otros patógenos o vacunas, lo que las hace más susceptibles a otras infecciones. Por otro lado, los cambios degenerativos causados por los FAdV en órganos linfoides clave, como el bazo y la bolsa de Fabricio, comprometen la respuesta inmunitaria tanto celular como humoral. Este compromiso del sistema inmunitario aumenta la posibilidad de infección con otros patógenos aviares.


En este aspecto, es esencial considerar que las infecciones por FAdV con frecuencia se asocian con coinfecciones con agentes inmunosupresores, como la enfermedad de Gumboro o la anemia infecciosa de los pollos. Estas coinfecciones exacerban aún más la inmunosupresión y aumentan la gravedad de la enfermedad.
Abordaje para el control de las infecciones por Adenovirus Aviares
La estrategia para un enfoque adecuado debe considerar un abordaje integral que incluya aspectos clave como:
- Minimizar la circulación y contaminación de los sistemas de producción: ejecutar prácticas de higiene y bioseguridad estrictas en las granjas para reducir las posibilidades de infección. Esto incluye limpieza y desinfección exhaustivas, control del movimiento de visitantes y vehículos, uso de ropa y calzado especiales, y control de roedores e insectos. En los casos donde se han detectado FAdV en el sistema de producción, se deben implementar acciones para reducir la carga viral en las instalaciones mediante intervenciones sobre el ambiente donde se alojarán las aves (tratamiento y reemplazo de cama, desinfección integral de los galpones, etc.).
- Minimizar el estrés de las aves: todos los factores ambientales y de manejo que tengan capacidad de inducir estrés en las aves deben considerarse potenciales “disparadores” de la enfermedad ante eventuales desafíos por FAdV. Existen múltiples antecedentes que ponderan el impacto del estrés térmico y el efecto de la elevada densidad de alojamiento ante eventuales infecciones por FAdV.
- Alojamiento de aves inmunocompetentes: las estrategias para el adecuado control de otros agentes inmunosupresores infecciosos (enfermedad de Gumboro, anemia infecciosa de los pollos, enfermedad de Marek, reovirosis aviar) y no infecciosos (micotoxinas y factores antinutricionales) son determinantes para el adecuado control de infecciones por FAdV. Es necesario alojar lotes de aves con capacidad para generar respuestas inmunes robustas y consistentes, para lograr el control efectivo de los desafíos de campo.
- Diagnóstico rápido y preciso: ante la sospecha de desafíos por FAdV, es fundamental implementar programas de monitoreo para detectar y caracterizar los serotipos de FAdV presentes en la región. El correcto diagnóstico es crucial para un adecuado control de los desafíos, ya que es el primer elemento a considerar para seleccionar e implementar programas de control adecuados.
- Aumentar la resistencia de las aves a la infección: la vacunación de las reproductoras es un método relevante para controlar las infecciones por FAdV en la progenie, asegurando la transferencia de anticuerpos maternos a todos los individuos que componen un lote. Luego de la administración de vacunas inactivadas a gallinas reproductoras, se induce la producción de anticuerpos circulantes que bloquean la transmisión vertical de FAdV de las madres a la progenie y retrasan la probabilidad de infección durante las primeras semanas de vida de los pollos. Para que la estrategia se adapte a la epidemiología de la enfermedad, se deben utilizar vacunas que contengan los serotipos prevalentes en la región.
Las evaluaciones realizadas en condiciones experimentales y los antecedentes de campo evidencian que la definición e implementación de programas con una visión global y con perspectiva integradora (manejo, prevención, diagnóstico, aspectos nutricionales, condiciones de alojamiento, etc.) para el control de los desafíos por Adenovirus Aviares permiten minimizar el impacto de la enfermedad sobre el desempeño de las aves y, por lo tanto, sobre las consecuencias económicas de los Adenovirus Aviares en la industria avícola.
Fuentes:
- Harrach, B., Z. L. Tarjan, and M. Benk}o. 2019. Adenoviruses across the animal kingdom: a walk in the zoo. FEBS Lett. 593:3660–3673.
- Hess, M. 2017. Commensal or pathogen – a challenge to fulfil Koch’s Postulates. Br. Poult. Sci. 58:1–12.
- Jaffery, M. S. 1988. A treatise on Angara disease (hydropericardium pulmonary oedema-hepatonephritis syndrome). J. Pak. Vet. Med. Association 34:1–33.
- Liu, Y., et al. 2016. Genetic characterization of novel fowl aviadenovirus 4 isolates from outbreaks of hepatitis hydropericardium syndrome in broiler chickens in China. Emerg. Microbes Infect. 5:e117.
- Mase, M., and K. Nakamura. 2014. Phylogenetic analysis of fowl adenoviruses isolated from chickens with gizzard erosion in Japan. J. Vet. Med. Sci. 76:1535–1538.
- Matos, M., et al. 2018. Pancreatitis is an important feature of broilers suffering from inclusion body hepatitis. Avian Dis. 62:57–64.
- McFerran, J. B., and J. A. Smyth. 2000. Avian adenoviruses. Rev. Sci. Tech. 19:589–601.
- Schachner, A., et al. 2018. Fowl adenovirus-induced diseases and strategies for their control. Avian Pathol. 47:111–126.
- Zhao, J., et al. 2015. Pathogenicity and complete genome characterization of fowl adenoviruses. PLoS One 11:e0161744.


